上海交通大学口腔医学院蒋欣泉团队揭示骨骼发育中破骨细胞谱系分化过程的“刹车器”
形成骨的成骨细胞与溶解吸收骨的破骨细胞(骨的两个主要细胞成分)之间的协调是维持骨骼的功能和稳态的重要细胞基础。其中,破骨细胞起源于骨髓,参与骨发育、改建和重建过程等重要生理过程,其分化功能异常导致骨质疏松,骨质硬化,骨坏死、佩吉特氏骨病等。因此,明确破骨细胞分化发育过程中的谱系分化的分子生物学调控机制,可为人类的骨骼系统相关疾病的治疗,以及促进骨再生修复提供重要的治疗线索。

前期研究表明溴结构域蛋白9 (BRD9),作为非典型染色质重塑BAF复合物(ncBAF)的重要组成亚基,是造血系统相关疾病的重要靶分子。然而,BRD9介导的染色质重塑功能在破骨细胞谱系分化与骨稳态调节中的作用仍不清楚。近日,上海交通大学口腔医学院、上海交通大学医学院附属第九人民医院蒋欣泉教授课题组,针对该问题于Nature子刊Nature Communications杂志,在线发表了题为“BRD9-mediated chromatin remodeling suppresses osteoclastogenesis through negative feedback mechanism”的研究论文。
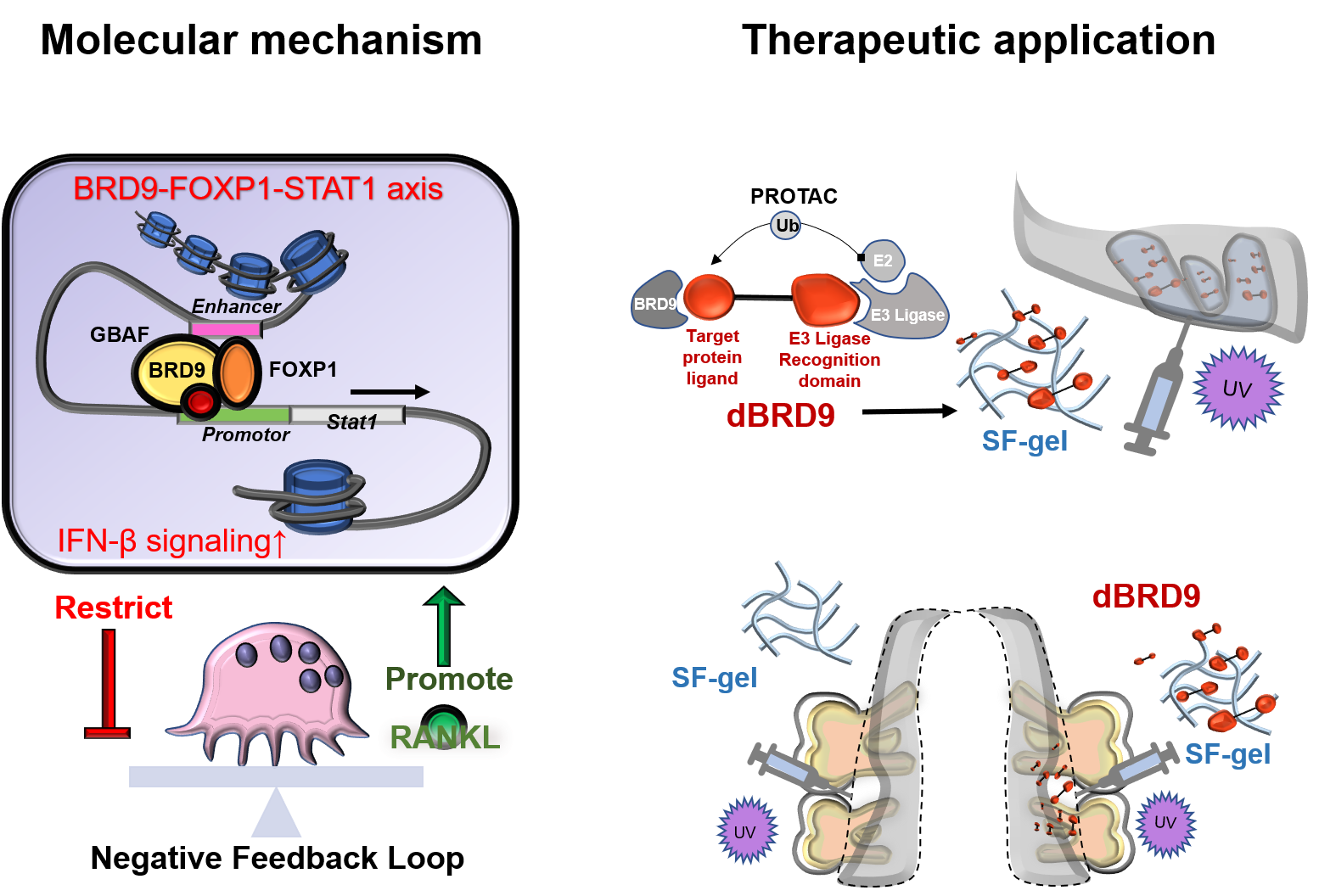
该研究中,作者首先构建了髓系条件性敲除Brd9的转基因小鼠,发现BRD9缺失后,破骨细胞的分化显著加速,并引起骨量的明显减少。为进一步探讨BRD9调节破骨细胞分化的分子机制,作者通过RNA-seq、ChIP-seq以及ATAC-seq多组学联合分析,以及相关的细胞分子实验,验证发现转录因子Foxp1作为BRD9协同作用蛋白之一,共同参与Stat1的基因激活转录,从而介导下游IFN-β信号通路的激活,在破骨细胞分化过程中起到限速“刹车器”作用。最后,作者设计了一种口腔拔牙创局部药物递送系统,将BRD9降解剂与可注射光固化丝蛋白水凝胶结合,有效缓解了双磷酸盐相关性颌骨坏死。鉴于BRD9的降解可同时抑制巨噬细胞的炎症反应,该递送系统在局部急性侵袭性牙周炎模型中,亦可通过降低局部炎症反应及其诱导的破骨细胞活化,有效缓解了局部急性骨丧失。综上,该研究揭示了BRD9-FOXP1-STAT1轴在破骨细胞形成过程中发挥重要的负反馈调节作用,拓展了BRD9介导的染色质重塑、经典转录因子和经信号通路,以及骨-免疫环路稳态的共同调控网络在髓系谱系分化中的功能,并为相关骨组织疾病的治疗提供了新的靶点和治疗策略。
该研究的第一作者杜佳慧博士,毕业于上海交通大学,现上海交通大学医学院附属第九人民医院口腔修复基地住院医师,曾于美国南加州大学牙学院访问学习,2021年入选上海市浦江人才计划,2022年获国家自然科学青年基金项目资助,研究方向聚焦口腔颅颌面组织发育和再生相关表观遗传调控分子生物学机制及再生修复应用,相关学术成果以第一作者发表于Nature Communications,Cell Reports,Development,Journal of Dental Research等杂志。上海交通大学医学院2022级致远荣誉计划直博生刘宜立为该论文的共同第一作者。该研究完成于上海口腔医学先进技术与材料工程技术研究中心和口腔发育再生与功能修复实验室。