首都医科大学基础医学院李晓光/杨朝阳教授团队《Signal Transduct Target Ther》发文阐述一种促进视神经再生的生物活性材料
近日,首都医科大学基础医学院神经生物学系李晓光教授、杨朝阳教授团队联合暨南大学苏国辉院士在《Signal Transduction and Targeted Therapy》杂志发表题为“Regeneration and functional recovery of the completelytransected optic nerve in adult rats by CNTF-chitosan”的研究论文。该研究使用生物活性材料【睫状神经营养因子(CNTF)-壳聚糖】促进了成年大鼠视神经的长距离再生并恢复了视觉功能,为临床转化奠定了良好的基础。基础医学院神经生物学系刘晓博士和北京航空航天大学医学科学与工程学院郝飞博士为共同第一作者,李晓光教授、苏国辉院士、杨朝阳教授为共同通讯作者。

视神经再生是国际上尚未解决的重大医学难题。外伤、肿瘤、缺血、出血、青光眼、神经退化及炎性疾病均可导致视神经的损伤。在视神经再生基础研究领域,国内外研究者主要聚焦于提高节细胞轴突的再生能力以及克服损伤区的抑制性环境。通过基因编辑的手段提高节细胞哺乳动物雷帕霉素靶蛋白(mTOR)的表达能显著促进其轴突再生,但再生的轴突不能越过视交叉且存在肿瘤形成的风险。单独克服损伤区的抑制性环境诱发的节细胞轴突再生效果甚微。因此,研究者需要寻找新的促进视神经再生的方法。组织工程修复神经系统损伤是目前研究的热点,在周围神经损伤和脊髓损伤中已经展现出巨大的应用前景。李晓光/杨朝阳教授团队将20多年使用生物活性材料修复脊髓损伤的经验和苏国辉院士团队40多年修复视神经损伤的经验进行优化整合,共同探讨生物活性材料是否能修复视神经损伤。
李晓光/杨朝阳教授团队研发了新型生物活性材料(CNTF-壳聚糖)。此生物活性材料能在生理温度下持续释放CNTF长达12周。团队使用成年大鼠视神经完全离断生物活性材料吻合模型,探讨CNTF-壳聚糖对视神经再生的促进作用。神经示踪技术、免疫荧光技术表明,CNTF-壳聚糖能促进视网膜节细胞轴突长距离再生,通过损伤区及视交叉并到达脑内视觉核团。透射电镜显示新生的轴突可重新形成髓鞘。运用免疫荧光技术及免疫电镜技术表明,节细胞新生的轴突能在外侧膝状体中重新形成突触连接。视觉电生理及视觉功能检测表明,新生的视觉通路能够执行视觉功能。此外,CNTF-壳聚糖对视网膜节细胞也具有良好的保护作用。
此研究可较快向临床转化。CNTF-壳聚糖也有希望应用于青光眼的治疗中。
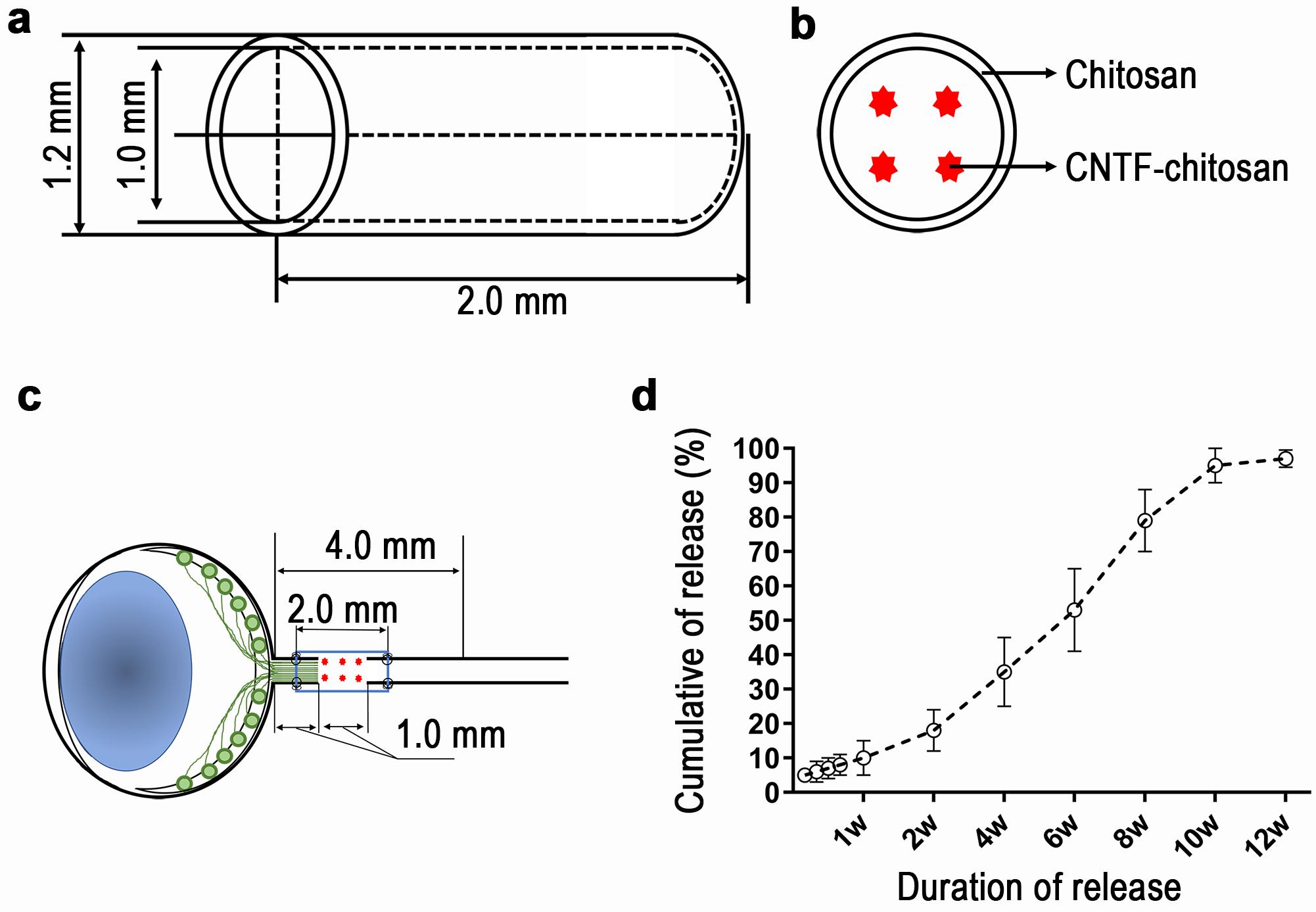
CNTF-壳聚糖植入示意图及CNTF-壳聚糖的体外释放曲线
该项研究得到了科技部重点研发计划(Grants 2017YFC1104001, 2017YFC1104002)、国家自然科学基金(Grants 31730030, 81941011, 31971279, 31771053, 31900749,31650001, 31320103903, 31670988)、北京市科委项目(Grant Z181100001818007)、北京市自然科学基金(Grant 7214301)等项目的资助。

李晓光,首都医科大学基础医学院教授、博士生导师。主要从事应用组织工程修复中枢神经损伤机理和临床转化研究。主持和完成科技部863、国家重点研发计划、国家自然科学基金重点项目等。在国际著名期刊《PNAS》《STTT》《Biomaterials》等发表论文30余篇,获国家发明专利多项,获“2012年全国百篇优秀博士学位论文指导老师”及“2018年高等学校科学研究优秀成果-自然科学一等奖”。

杨朝阳,首都医科大学基础医学院教授、博士生导师。主要从事应用组织工程学方法修复中枢神经系统损伤研究。主持完成科技部重点研发计划(子课题)、国家自然科学基金面上项目等多项国家级科研项目。在《PNAS》《STTT》《Biomaterials》等期刊上发表论文30余篇。获“2018年高等学校科学研究优秀成果-自然科学一等奖”、“2012年全国百篇优秀博士学位论文”、“2018年中华医学会-医学科学技术三等奖”。