北京友谊医院尤红教授团队《Hepatology》发文阐述肝纤维化分子分型
近日,首都医科大学附属北京友谊医院尤红教授团队在《Hepatology》发表题为“Matrisome gene-based subclassification of patients with liver fibrosis identifies clinical and molecular heterogeneities”的研究论文,首次报道了基于基质基因谱可实现对具有不同临床和生物学特征的肝纤维化患者亚分型,该分子分型方法有助于推动肝纤维化传统病理诊断向分子病理诊断的转变,为精准诊治肝纤维化提供新方向。首都医科大学附属北京友谊医院陈巍副研究员与孙亚朦副研究员为共同第一作者,尤红教授(末位通讯)和美国伊利诺伊大学芝加哥分校Natalia Nieto教授为共同通讯作者。

多种病因损伤刺激可导致细胞外基质过度交联沉积形成肝纤维化,而肝纤维化是诱发肝癌的主因。目前临床上肝纤维化治疗以病因控制为主,尚无特效药。然而,大量的临床研究表明,病因控制仅有部分患者肝纤维化逆转。如何区分这些患者纤维化转归并阐明其分子机制是核心科学问题。
尤红教授团队长期从事肝纤维化的基础与临床研究,通过对大量肝纤维化转录组谱的综合分析,发现了一个不受病因扰动的肝纤维化特异性基质基因集(LFMG)。基于LFMG可从分子水平上精准评估肝纤维化的细微变化。另外,基于LFMG基质基因集可将具有相同组织学纤维化分期的患者亚分类为LFMGLow和LFMGHigh,两组患者具有不同的病理特征、肝脏硬度、肝内分子信号活性以及细胞景观,这可能是病因控制后不同肝纤维化患者临床获益不同的潜在原因。进一步单细胞测序分析结果表明,MFAP4+活化的肝星状细胞亚型(MFAP4+aHSC)是LFMG基质基因集表达及失调的主要细胞来源,也是驱动肝纤维化患者LFMGLow和LFMGHigh分子分型的细胞学基础。
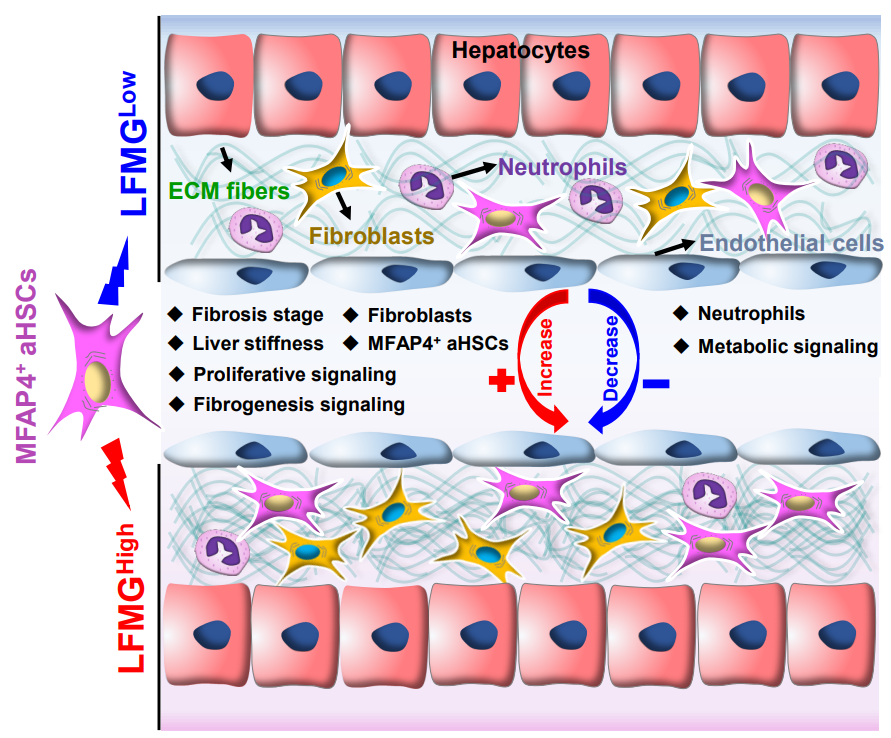
图. MFAP4+活化肝星状细胞衍生的LFMG特征基质基因集亚分类具有不同临床和分子特征的肝纤维化患者示意图
该研究首次提出了基于LFMG基质基因集的肝纤维化分子分型系统,可为肝纤维化患者的精准诊断、预后分层、治疗指导及药物研发提供新思路,进而有望为更多的肝纤维化患者带来临床获益。
该研究得到国家自然科学基金(82170613,81970524,82130018,81800534)和“十三五”国家科技重大专项(2018ZX10302204)等项目资助。

尤红,首都医科大学附属北京友谊医院肝病中心教授,主任医师,研究员,消化内科博士研究生导师。现任中华医学会肝病学分会副主任委员,亚太肝病学会副秘书长兼执行委员。研究方向为消化系统肝脏疾病,特别是慢性肝病肝纤维化。牵头国家十二五和十三五重大传染病专项中“逆转乙肝纤维化肝硬化及阻断疾病进展的优化治疗”项目,主持国家自然基金重点项目和面上项目等;在《J Hepatol》《Hepatology》《Am J Gastroenterol》《Clin Gastroenterol Hepatol》等杂志发表SCI论文180余篇;获得国家百千万人才项目,教育部新世纪优秀人才项目;获得华夏医学科技奖一等奖(第一完成人)和北京市科技进步一等奖(第二完成人)。